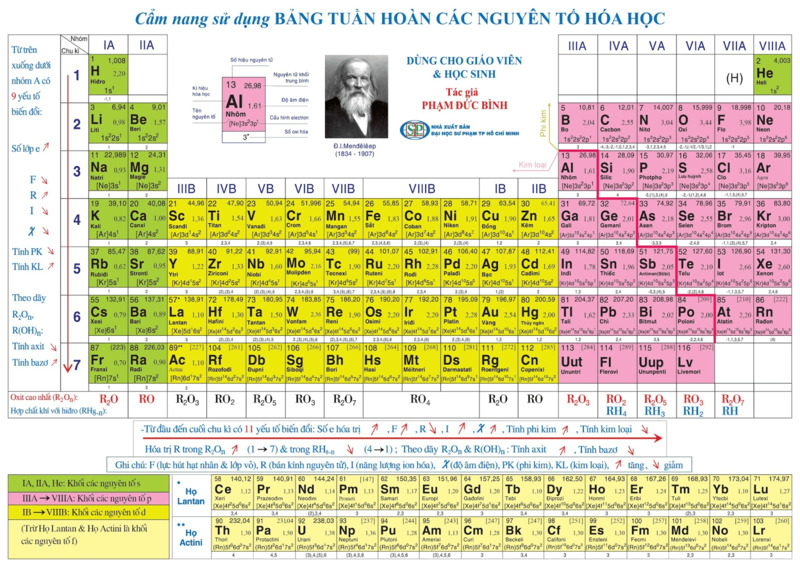
Bảng tuần hoàn hóa học, chắc hẳn trong mỗi chúng ta, ai cũng đã từng nghe và sử dụng bảng tuần hoàn này. Trong hóa học, bảng tuần hoàn các nguyên tố hóa học là thứ không thể thiếu được, bởi chúng đóng vai trò vô cùng quan trọng. Vậy bảng tuần hoàn hóa học là gì? Chúng xuất hiện từ bao giờ và có cấu tạo, ý nghĩa như thế nào? Hãy cùng tìm hiểu nhé.
Lịch sử hình thành và phát triển của bảng tuần hoàn hóa học
Lịch sử hình thành và phát triển của bảng tuần hoàn hóa học
Vào năm 1869, bảng tuần hoàn hóa học được biên soạn bởi người Nga – Dmitri Mendeleev. Tuy nhiên, khi ấy vẫn có những khoảng trống do các nguyên tố vẫn chưa được khám phá hết..
Sau đó, vào năm 1870, Nhà hóa học người Đức Lothar Meyer đã tạo ra một phiên bản của bảng tuần hoàn tương tự như của Mendeleev vào năm 1870. Và những khoảng trống cho các nguyên tố cũng chưa được khám phá hết, nhưng ông chưa bao giờ dự đoán tính chất của chúng.
Mendeleev và Meyer đã nhận được Huân chương Davy năm 1882 do Hiệp hội Hoàng gia Luân Đôn trao tặng. Các nguyên tố bao gồm gali (1875), scandi (1879) và germanium (1886), do Mendeleev dự đoán sau đó đã xác minh và bảng tuần hoàn của ông đã được công nhận rộng rãi.
Năm 1955, để vinh danh Mendeleev, nguyên tố thứ 101 được đặt tên là mendelevium.
Năm 1869, bảng tuần hoàn của Mendeleev được viết bằng tiếng Nga, với tiêu đề có nghĩa là “Thí nghiệm về một hệ thống các nguyên tố… dựa trên trọng lượng nguyên tử và sự tương đồng hóa học của chúng”.
Khi các nguyên tố mới được tìm thấy thì bảng tuần hoàn cũng phải trải qua nhiều lần điều chỉnh. Tuy nhiên, các hình thức hiển thị cơ bản thì đều được giữ nguyên như thiết kế ban đầu của Mendeleev.
Bảng tuần hoàn hóa học là gì?
Bảng tuần hoàn hóa học hay bảng tuần hoàn Mendeleev là phương pháp dạng bảng, biểu thị lên các nguyên tố hóa học Dmitri Mendeleev người Nga.
Thông thường, bảng tuần hoàn hóa học sẽ biểu thị nguyên tố hóa học theo cách sắp xếp cấu hình electron, số hiệu nguyên tử của nguyên tố và quy luật tuần hoàn khác. Dựa vào giá trị của bảng tuần hoàn hóa học, ta có thể tính toán tính chất hóa học của một nguyên tố dựa trên vị trí của nó.
Cấu tạo bảng tuần hoàn hóa học
Một bảng tuần hoàn hóa học sẽ có cấu tạo bao gồm: ô nguyên tố, chu kỳ và nhóm nguyên tố.
Ô nguyên tố
Thể hiện các thông tin về số hiệu nguyên tử, tên nguyên tố, ký hiệu hóa học, nguyên tử khối của nguyên tố hóa học trong ô.
Trong đó, số hiệu nguyên tử thể hiện số thứ tự của nguyên tố đó trong bảng tuần hoàn. bên cạnh đó, số hiệu nguyên tử có số trị bằng số đơn vị của điện tích hạt nhân và bằng số electron trong nguyên tử.
Chu kỳ
Chu kỳ sẽ biểu hiện dãy các nguyên tố hóa học được xếp theo chiều điện tích hạt nhân tăng dần và các nguyên tử có cùng số lớp electron.
Trong đó: STT của chu kỳ = số lớp electron
Trong bảng tuần hoàn nguyên tố hóa học có tất cả 7 chu kỳ, chu kỳ nhỏ sẽ bao gồm chu kỳ 1, 2, 3, còn chu kỳ 4, 5, 6, 7 gọi là chu kỳ lớn.
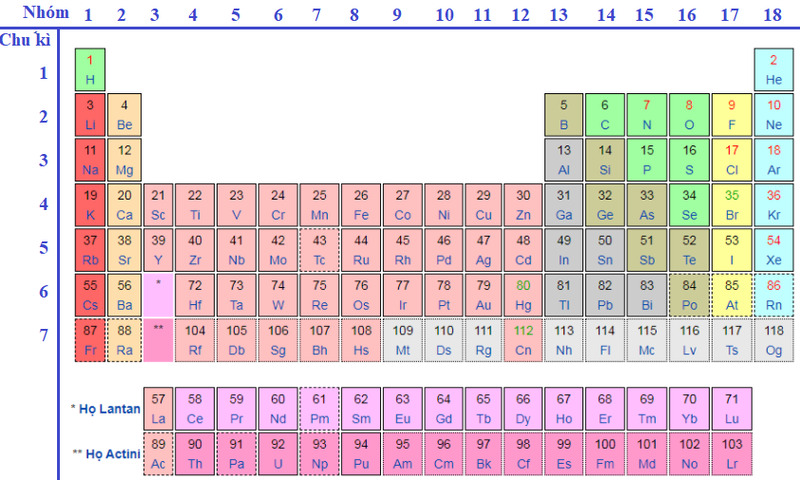
Chu kỳ sẽ biểu hiện dãy các nguyên tố hóa học
-
Chu kỳ 1: Có 2 nguyên tố là H và He, đều là nguyên tố có 1 lớp electron trong nguyên tử. Điện tích hạt nhân sẽ tăng từ H1+ tới He 2+.
-
Chu kỳ 2: Với 8 nguyên tố từ Li đến Ne đều có 2 lớp electron. Điện tích hạt nhân sẽ tăng từ Li 3+ tới Ne 10+.
-
Chu kỳ 3: Bao gồm 8 nguyên tố từ Na đến Ar đều có 3 lớp electron. Trong đó, điện tích hạt nhân và nguyên tử tăng từ Na 11+ đến Ar 18+.
-
Chu kỳ 4 và chu kỳ 5: Mỗi chu kỳ sẽ có 18 nguyên tố, bắt đầu từ kim loại kiềm K là 19+ và Rb 37+, kết thúc là Xe 54+ và Kr 36+.
-
Chu kỳ 6: Có 32 nguyên tố, bắt đầu từ kim loại kiềm Cs 55+ và kết thúc là Rn 86+.
-
Chu kỳ 7: Chưa hoàn thành.
Nhóm nguyên tố
Những nguyên tử có cùng số electron lớp ngoài cùng sẽ được tập hợp lại do có tính chất tương tự nhau và được xếp thành cột theo chiều tăng dần của điện tích hạt nhân từ dưới lên trên.
Mỗi cột trong bảng tuần hoàn hóa học sẽ ứng với từng nhóm hoặc họ tương ứng, các chất có cùng tính chất hóa học sẽ xếp trong cùng 1 nhóm. Và hiện nay, trên bảng tuần hoàn tiêu chuẩn có 18 nhóm khác nhau.
Trong bảng tuần hoàn có 2 loại nhóm lớn là A và B.
Nhóm A bao gồm các nguyên tố s và p nên số thứ tự nhóm A bằng số electron lớp ngoài cùng.
Bên cạch đó, nhóm B gồm các nguyên tố d và f. Chúng có cấu hình e lớp ngoài cùng là \((N-1)d^x Ns^y\) và số thứ tự trong nhóm sẽ bằng x+y.
Trong trường hợp x+y nằm trong khoảng 8-10 thì sẽ thuộc nhóm VIIIB, x+y>10 thì thuộc nhóm (x+y-10)B
Ý nghĩa quan trọng của bảng tuần hoàn hóa học
Trong bảng tuần hoàn, mỗi vị trí, mỗi yếu tố đều có sự liên kết chặt chẽ với nhau. Chúng ta có thể dựa vào vị trí để suy ra được cấu tạo vào tính chất của nguyên tố đó. Hay dựa vào cấu tạo để suy ra tính chất và vị trí của chúng.
Vị trí của nguyên tố hóa học
Khi biết được vị trí của nguyên tố hóa học, ta có thể suy ra được cấu tạo và tính chất của nguyên tố hóa học đó.
Ví dụ: Khi ta biết được nguyên tố X có số hiệu nguyên tử là 16, thuộc chu kỳ 3, nhóm VIA, ta có thể suy ra được:
-
Điện tích hạt nhân của nguyên tố X là 16+ và nguyên tố này có 16 electron (số hiệu nguyên tử là 16)
-
Do thuộc chu kỳ 3 nên nguyên tố X có 3 lớp electron.
-
Thuộc nhóm VIA nên lớp ngoài cùng của nguyên tố X có 6 electron.
Cấu tạo nguyên tử
Ta có thể suy ra được vị trí và tính chất của nguyên tố hóa học trong bảng tuần hoàn, dựa trên cấu tạo nguyên tử của nguyên tố hóa học.
Ví dụ: Khi thông tin chó biết nguyên tố Y có điện tích hạt nhân là 12+, có 3 lớp electron và lớp ngoài cùng có 2 electron, ta có thể suy ra được:
-
Do điện tích hạt nhân 12+ nên nguyên tố Y nằm ở ô thứ 12, thuộc chu kỳ 3 (có 3 lớp electron),
-
Ngoài ra, lớp ngoài cùng có 2 electron nên nguyên tố Y thuộc nhóm IIA trên bảng tuần hoàn.
-
Nguyên tố Y là kim loại do nằm ở đầu chu kỳ.
Hướng dẫn đọc bảng tuần hoàn hóa học chính xác
Để sử dụng bảng tuần hoàn hóa học một cách chính xác và hiệu quả, bạn cần nắm được những thông tin cơ bản sau:
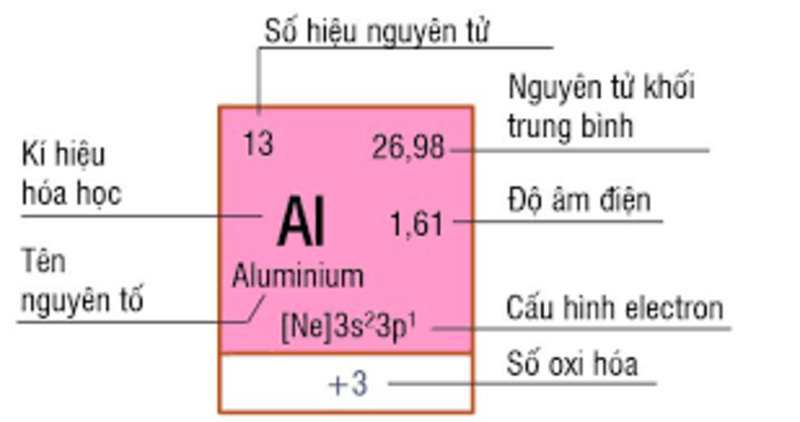
Hướng dẫn đọc bảng tuần hoàn hóa học chính xác và hiệu quả
-
Số nguyên tử: còn được biết đến là số proton của nguyên tố hóa học. Thể hiện số proton có thể tìm thấy trong hạt nhân của một nguyên tử. Đồng thời, là số điện tích hạt nhân. Đặc biệt là số nguyên tử giúp xác định được duy nhất 1 nguyên tố.
-
Nguyên tử khối trung bình: là số NTK trung bình của hỗn hợp các đồng vị, tính đến tỷ lệ phần trăm số nguyên tử tương ứng.
-
Độ âm điện: thể hiện khả năng hút electron của nguyên tử khi tạo liên kết hóa học. Nếu độ âm điện của nguyên tử nguyên tố càng lớn thì tính phi kim càng mạnh và ngược lại.
-
Cấu hình electron: khi nhìn vào đây, ta có thể nắm được sự phân bố các electron trong lớp vỏ nguyên tử ở những trạng thái năng lượng khác nhau.
-
Số oxi hóa: thông qua số oxi hóa, chúng ta có thể nhận biết được số electron trao đổi khi một chất bị khử hoặc bị oxi hóa.
-
Ký hiệu hóa học: đây là tên viết tắt của một nguyên tố trong bảng tuần hoàn hóa học.
-
Tên nguyên tố: là một chất hóa học tinh khiết, được phân biệt bởi số hiệu nguyên tử, là số lượng proton có trong hạt nhân.
Một số nguyên tắc sắp xếp trong bảng tuần hoàn hóa học
Thứ tự sắp xếp trong bảng tuần hoàn hóa học thể hiện tương đối rõ ràng khả năng hoạt động hóa học của các nguyên tố. Để nắm được nguyên tắc sắp xếp, bạn có thể tham khảo những yếu tố sau:
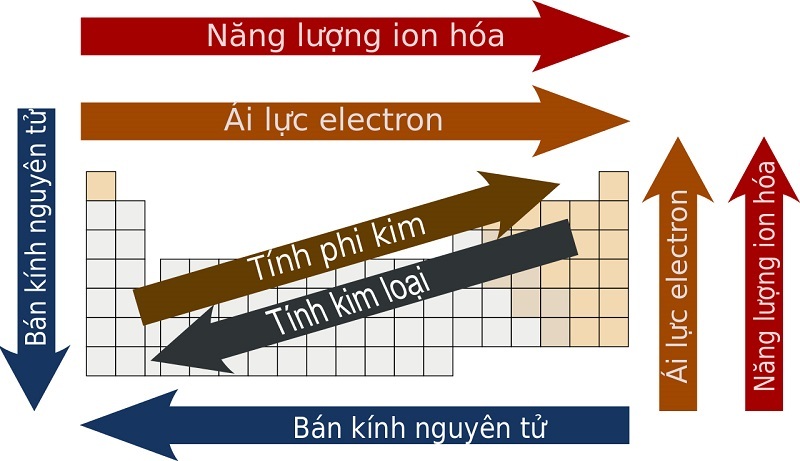
Nguyên tắc sắp xếp trong bảng tuần hoàn hóa học
-
Tính kim loại sẽ giảm dần theo thứ tự từ trái sang phải.
-
Tính phi kim tăng dần theo hướng từ trái sang phải.
-
Đối với các nhóm nguyên tố hóa học giảm dần theo chiều từ trên xuống dưới sẽ biểu thị khả năng hoạt động hóa học và tính chất đặc trưng của chúng
-
Năng lượng ion hóa và ái lực electron của các nguyên tố tăng dần từ trái sang phải và dưới lên trên
-
Bán kính nguyên tử giảm dần theo hướng từ trên xuống dưới, từ phải sang trái.
Gợi ý những phương pháp ghi nhớ bảng tuần hoàn hóa học
Có rất nhiều cách để có thể ghi nhớ được bảng tuần hoàn hóa học. Dưới đây, sẽ chia sẻ một vài phương pháp ghi nhớ nhanh, hiệu quả.
Ghi nhớ bằng cách truyền thống
Trước khi sử dụng bảng tuần hoàn, bạn cần phải nắm được số nguyên tử, nguyên tử khối trung bình, độ âm điện, số oxi hóa, cấu hình electron, tên ký hiệu, ký hiệu hóa học. Tất cả các thông tin trên đều có trong ô nguyên tử của bảng tuần hoàn
Để ghi nhớ theo cách truyền thống bạn cần:
-
Dán bảng tuần hoàn hóa học ở những khu vực dễ nhìn thấy.
-
Làm thẻ ghi chú cho mỗi nguyên tố, giống như làm một tập flashcard.
-
Mỗi ngày học vài nguyên tố để não có thể ghi nhớ được lâu dài.
Phương pháp ghi nhớ hiệu quả
Theo bài ca hóa trị:
Đây là một trong những phương pháp tổng hợp kiến thức hóa học, thông qua những câu thơ và bài ca dao, giúp việc học không bị nhàm chán và dễ dàng học thuộc.

Phương pháp ghi nhớ hiệu quả theo bài ca hóa trị
Dãy hoạt động của kim loại:
Dãy hoạt động hóa học của kim loại được sắp xếp lần lượt: Na, F, Ca, Mg, Al, Zn, Fe, Ni, Sn, Pb, H, Cu, Hg, Ag, Pt, Au.
Để ghi nhớ 16 nguyên tố hóa học này trong dãy hoạt động của kim loại, bạn chỉ cần nhớ câu nói sau:
“ Khi nào cần mua áo giáp sắt nhớ sang phố hỏi cửa hàng Á Phi Âu”
Trên đây là toàn bộ những thông tin cơ bản liên quan đến bảng tuần hoàn hóa học mà Chemical muốn chia sẻ đến bạn. Với những kiến thức liên quan đến cấu tạo, ý nghĩa, cách đọc và mẹo ghi nhớ bảng tuần hoàn. Mong rằng bài viết này sẽ đã giúp bạn hiểu hơn và bảng tuần hoàn hóa học và cách sử dụng học liệu này một cách hiệu quả nhất